Perbezaan Antara Alkanes dan Alkene | Alkanes vs Alkene
Perbezaan Utama - Alkanes vs Alkenes
Alkanes dan Alkenes adalah dua jenis keluarga hidrokarbon yang mengandungi karbon dan hidrogen dalam struktur molekulnya. Perbezaan utama antara Alkanes dan Alkenes ialah struktur kimia mereka; Alkana adalah hidrokarbon jenuh dengan rumus molekul umum C n H 2n + 2 dan alkenes dikatakan sebagai kumpulan hidrokarbon tak tepu kerana ia mengandungi ikatan berganda antara dua karbon atom. Mereka mempunyai formula molekul umum C n H 2n.
Apa Alkanes?Alkana mengandungi hanya satu ikatan antara atom Karbon dan hidrogen (ikatan C-C dan ikatan C-H). Oleh itu, mereka dipanggil "hidrokarbon jenuh". Menurut model hibridisasi orbit, semua atom karbon di Alkenes mempunyai hibridisasi SP
3 . Mereka membentuk ikatan sigma dengan atom hidrogen, dan molekul yang dihasilkan mempunyai geometri tetrahedron. Alkana boleh dibahagikan kepada dua kumpulan mengikut susunan molekul mereka; alkana akiklik (C n H 2n. +2 ) dan alkana siklik (C n H 2n ).

Alkenes adalah hidrokarbon, yang mengandungi ikatan berganda karbon-karbon (C = C).
"Olefins" adalah nama lama yang digunakan untuk merujuk kepada keluarga alkena. Ahli keluarga terkecil adalah etana (C 2 H 4 ); ia dipanggil olefian t gas (Dalam Bahasa Latin: ' oleum' bermaksud 'minyak' + 'facere' Ini kerana tindak balas antara C 2 H 4 dan Klorin memberikan C 2 H 2 Cl 2 minyak.

Struktur Kimia Alkana dan Alkenes
Alkana:
Alkana mempunyai formula molekul umum C n H 2n + 2. Methane (CH 4 ) adalah alkane terkecil. - diff Artikel Tengah sebelum Jadual ->
Nama| Rumus kimia | Struktur aciklik | Methane |
| CH | 4 CH | 4 Ethane C |
| 2 | H 6 CH 3 | CH 3 Propane C |
| 3 | H 8 CH 2 | CH 3 Butana C 4 H |
| 10 | CH 3 CH 2 CH | 2 CH 3 Pentane C 5 H 12 |
| CH | 2 CH 2 CH | 2 CH 3 Hexane C 6 H 14 CH 3 CH |
| 2 | CH 2 CH 2 | CH 2 CH 3 Heptane C 7 H 16 CH 3 CH |
| 2 | CH 2 CH 2 CH | 2 CH 2 CH 3 Octane C 8 H 18 CH 3 CH 3 |
| CH | 2 CH 2 CH | 2 CH 2 CH 3 CH 3 Alkenes: Alkenes mempunyai formula kimia umum C n H 2n .Alkenes dianggap sebagai hidrokarbon tak tepu kerana ia tidak mengandungi bilangan maksimum atom hidrogen yang boleh dimiliki oleh molekul hidrokarbon. Nama Rumus kimia Struktur Ethene |
C 2 H 4 CH 2 =
| CH | 2 | Propene |
| C | 3 H 6 CH | 3 CH = CH 2 Butene |
| C | 4 CH 2 CHCH | 2 CH 3, CH |
| 3 | CH = CHCH 2 CHCH 2 | CH 2 CH 3 CH = CHCH 2 CH 3 Hexene C |
| 6 | H 12 CH 2 = CHCH | 2 CH 2 CH 2 CH 3 CH 3 CH |
| 3 | CH 3 CH 2 | CH = CHCH 2 CH 3 Heptene C 7 H 2 CH 2 CH 2 CH 2 CH
3 CH < 2 CH 2 CH 2 CH 3 Sifat Kimia Alkanes dan Alkenes Alkanes: |
| Reaktiviti: | Alkanes tidak bereaksi terhadap banyak reagen kimia. Ini kerana bon Carbon-Carbon (C-C) dan Karbon - Hidrogen (C-H) agak kuat kerana atom Karbon dan Hidrogen mempunyai nilai elektronegativiti yang sama. Oleh itu, sangat sukar untuk memecahkan bon mereka, kecuali jika ia dipanaskan pada suhu yang cukup tinggi. Pembakaran: Alkana mudah terbakar di udara. Reaksi antara Alkana dengan Oksigen yang berlebihan dipanggil "pembakaran". Dalam tindak balas ini, alkana ditukar kepada Karbon dioksida (CO 2 | ) dan air. H 2n + (n + n / 2) O 2 → n CO 2 + nH 2 O C 4 H 10 + 13/2 O 2 → 4 CO 2 + 5H 2 O Air Karbon Dioksida Oksigen Butan Reaksi pembakaran adalah tindak balas eksotermik (mereka melepaskan haba). Akibatnya, alkana digunakan sebagai sumber tenaga. Alkenes: Reaktiviti: |
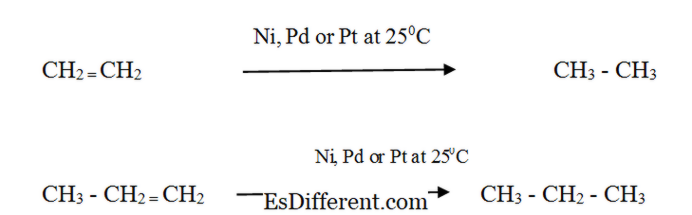
Alkenes bertindak balas dengan Hidrogen dengan kehadiran pemangkin logam halus dibentuk untuk membentuk alkane yang sesuai. Kadar reaksi sangat rendah tanpa pemangkin.
Hidrogenasi katalitik digunakan dalam industri makanan untuk menukar minyak sayur cair kepada lemak separuh pepejal dalam membuat lemak marjerin dan pepejal yang kukuh. Sifat-sifat Fizikal Alkana dan Alkenes
Bentuk
Alkana:
Alkana wujud sebagai gas, cecair dan pepejal. Metana, etana, propana dan butana adalah gas pada suhu bilik. Struktur tanpa heksana, pentana dan heptane adalah cecair. Alkana yang mempunyai berat molekul yang lebih tinggi adalah pepejal.
CH 4 ke C
4 H 10 adalah gas C 5 H 12 C 17 H
36 adalah cecair, dan Alkanes dengan berat molekul yang lebih tinggi adalah pepejal lembut Alkenes: Alkenes menunjukkan sifat fizikal yang serupa dari Alkane yang sepadan. Alkenes yang mempunyai berat molekul yang lebih rendah (C 2 H 4 toC 4 H
8) adalah gas pada suhu bilik dan tekanan atmosfera.Alkenes yang mempunyai berat molekul yang lebih tinggi adalah pepejal.
Kelarutan:
Alkana:
Alkana tidak larut dalam air. Mereka dibubarkan dalam pelarut organik bukan polar atau lemah polar.
Alkenes:
Alkenes adalah molekul yang relatif polar kerana ikatan C = C; oleh itu, mereka larut dalam pelarut bukan kutub atau pelarut rendah kutub. Air adalah molekul kutub dan alkenes sedikit larut dalam air.
Ketumpatan:
Alkana: Ketumpatan Alkana lebih rendah daripada ketumpatan air. Nilai ketumpatan mereka adalah hampir 0. 7 g mL
-1 , mengingat ketumpatan air sebagai 1. 0 g mL -1 . Alkenes: Kepekatan Alkenes lebih rendah daripada ketumpatan air. Titik didih:
Alkanes: Titik mendidih alkane tanpa biji meningkat dengan lancar kerana bilangan atom Karbon dan berat molekul semakin meningkat. Secara umum, alkana bercabang mempunyai titik didih yang lebih rendah berbanding dengan alkana tanpa biji, yang mempunyai bilangan atom karbon yang sama. Alkenes : Titik didih mirip dengan alkana yang sesuai dengan variasi yang kecil. Rujukan: CliffsNotes. (n. d.). Diperoleh pada 06 Julai 2016, dari sini. Sifat-sifat Fizikal Alkana. (2013). Diperoleh pada 06 Julai 2016, dari sini Zum Directory-modus. (n. d.). Diperoleh pada 06 Julai 2016, dari sini Sifat kimia Alkanes: Wizznotes. com- Percuma GCSE dan CXC: Tutorial, Kertas lalu dan Kuiz. (n. d.). Diperoleh pada 06 Julai 2016, dari sini
Polariti. (n. d.). Diperoleh pada 06 Julai 2016, dari sini
masa Dipole. (2013). Diperoleh pada 06 Julai 2016, dari sini isomer Struktural. (n. d.). Diperoleh pada 06 Julai 2016, dari sini Pengenalan kepada alkenes. (n. d.). Diperoleh pada 06 Julai 2016, dari sini Image Courtesy: "Nama Alkene" Oleh Chris Evans - (CC0) Wikimedia Commons "Coklat C4 hydrocarbons" Public Domain) melalui Wikimedia Commons


