Perbezaan Antara Phenyl dan Benzyl | Phenyl vs Benzyl
Phenyl vs Benzyl
Kedua-dua fenil dan benzil berasal dari benzena, dan biasanya dikelirukan oleh pelajar kimia. Phenyl adalah molekul hidrokarbon dengan formula C 6 H 5 , sedangkan benzil ialah C 6 H 5 CH 2 <; kumpulan tambahan CH 2 yang dilampirkan pada cincin benzena. Phenyl

6 H 5 . Ini berasal dari benzena, oleh itu, mempunyai sifat yang sama seperti bensin. Walau bagaimanapun, ini berbeza daripada benzena kerana kekurangan atom hidrogen dalam satu karbon. Oleh itu, berat molekul fenil ialah 77 g mol -1 . Phenyl disingkatkan sebagai Ph. Biasanya fenil dilampirkan kepada kumpulan fenil, atom, atau molekul lain (bahagian ini dikenali sebagai substituen, kumpulan R seperti dalam angka). Atom karbon fenil adalah sp2 yang hibridisasi seperti dalam benzena. Semua karbon boleh membentuk tiga ikatan sigma. Dua ikatan sigma dibentuk dengan dua karbohidrat yang bersebelahan, sehingga ia akan menimbulkan struktur cincin. Ikatan sigma yang lain terbentuk dengan atom hidrogen. Walau bagaimanapun, dalam satu karbon, dalam gelang, ikatan sigma ketiga terbentuk dengan atom atau molekul lain dan bukannya atom hidrogen. Elektron dalam orbital p bertindih antara satu sama lain untuk membentuk awan elektron yang disalirkan. Oleh itu, fenil mempunyai panjang ikatan C-C sama antara semua karbon, tanpa menghiraukan ikatan tunggal dan berganda. Panjang bon C-C ini adalah kira-kira 1. 4 Å. Cincin itu adalah planar dan mempunyai sudut 120 ° di antara ikatan di sekeliling karbon. Oleh sebab kumpulan phenyl substituen, polariti dan sifat kimia atau fizikal lain berubah. Sekiranya substituen menderma elektron ke awan elektron yang diselalogkan, mereka dikenali sebagai kumpulan penyumbang elektron (E. g. -OCH 3 , NH 2 ). Sekiranya substituen menarik elektron dari awan elektron, ia dikenali sebagai elektron yang mengeluarkan substituen. (E. g. -NO 2 , -COOH). Kumpulan fenil stabil kerana aromatiknya, jadi mereka tidak mudah menjalani pengoksidaan atau pengurangan. Selanjutnya, mereka adalah hidrofobik dan bukan kutub.
Formula benzyl ialah C
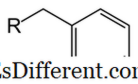
6 H 5 CH 2 . Ini juga merupakan derivatif benzena. Berbanding dengan fenil, benzil mempunyai kumpulan CH 2 yang dilekatkan pada cincin benzena. Bahagian molekul lain (kumpulan R seperti yang digambarkan dalam gambar) boleh dilampirkan kepada kumpulan benzyl melalui ikatan kepada atom karbon CH 2 . Kumpulan Benzyl disingkat sebagai "Bn". Berat molekul kumpulan benzil ialah 91 g mol -1 . Oleh kerana terdapat cincin benzena, kumpulan benzil adalah aromatik.Dalam mekanisme kimia organik, kumpulan Benzyl boleh dibentuk sama ada sebagai radikal, karbokation (C 6 H 5 CH 2 + ) atau carboanion C 6 H 5 CH 2 - ). Sebagai contoh, dalam tindak balas penggantian nukleofilik, radikal benzylic atau kation perantara terbentuk. Terdapat penstabilan yang lebih tinggi daripada perantaraan ini berbanding radikal alkil atau kation. Kereaktifan kedudukan benzylic adalah sama dengan kedudukan allylic. Kumpulan benzyl sering digunakan dalam kimia organik sebagai kumpulan perlindungan, terutama untuk melindungi kumpulan asid karboksilik atau kumpulan alkohol.
• Fenil molekul fenil ialah C
6 H 5 sedangkan dalam benzil, ia adalah C 6 H 5 CH < 2 . • Benzyl mempunyai kumpulan CH tambahan 2
berbanding fenil. • Dalam phenyl, cincin benzena dilekatkan secara langsung kepada molekul substituen atau atom, tetapi dalam benzil, kumpulan CH 2
membuat sambungan dengan molekul atau atom lain.




