Perbezaan antara Sigma dan Pi bond Perbezaan Antara
Apakah ikatan Sigma?
Ikatan Sigma adalah ikatan di antara atom-atom dalam molekul yang terbentuk di sepanjang paksi yang menyambung nuklei atom yang terikat.
Ikatan molekul
Molekul terbentuk apabila pertukaran atom atau elektron berkongsi melalui ikatan kimia. Pada dasarnya terdapat tiga jenis bon. Ikatan ionik, ikatan logam, dan ikatan kovalen. Dalam ikatan ionik, atom hanya akan menukar elektron supaya satu atom akan dikenakan secara positif dan yang lain dikenakan secara negatif, menyebabkan mereka tertarik oleh daya elektromagnetik. Dalam ikatan logam, elektron akan diedarkan secara seragam melalui seluruh molekul yang mewujudkan laut bebas, elektron-elektron yang disulingkan menyelubungi ion-ion bermuatan positif yang tertarik kepada elektron.
Dalam ikatan kovalen, elektron dikongsi dan cara yang dikongsi bersama adalah melalui awan kebarangkalian elektron, dan orbital di mana ia berada, bertindih dengan cara yang lebih kurang simetris.
Orbital dan ikatan sigma
Orbital adalah kawasan sekitar atom yang berkaitan dengan tahap tenaga tertentu. Elektron dalam orbital jauh dari nukleus akan mempunyai lebih banyak tenaga daripada elektron dalam orbital lebih dekat dengan nukleus. Apabila orbital satu atom bertindih dengan orbital dari atom lain, ia membentuk orbital molekul yang membolehkan ikatan molekul yang, tentu saja, membolehkan molekul.
Ikatan Sigma adalah jenis bon pertama yang akan membentuk antara atom. Dalam ikatan sigma, awan kebarangkalian elektron akan berada di sepanjang paksi yang menghubungkan nukleus atom terikat. Ikatan Sigma biasanya akan terbentuk apabila orbital s dari atom berbeza bertindih untuk membuat ikatan. Mereka akan sentiasa membentuk sepanjang paksi antara kedua-dua nukleus kerana orbit s disusun dalam sesuatu seperti sfera di sekeliling nukleus.
Ikatan Sigma dan orbitals sigma
Elektron yang membentuk ikatan sigma akan berada di dalam orbitals sigma dan dengan itu akan berada di sepanjang paksi yang menyambungkan inti atom terikat. Ikatan sigma boleh, bagaimanapun, stabil atau tidak stabil bergantung kepada sama ada elektron berada dalam orbital ikatan sigma atau orbital anti-ikatan. Orbital ikatan Sigma akan berada di ruang antara nukleus manakala orbital anti-ikatan akan berada di sepanjang paksi yang menyambungkan nukleus tetapi pada sisi atom bertentangan dengan ruang di antara mereka. Ikatan sigma akan stabil jika lebih banyak elektron berada dalam orbital ikatan dan tidak stabil jika lebih banyak berada dalam orbital antibonding atau jika terdapat bilangan elektron yang sama di kedua-duanya.
Apa ikatan Pi?
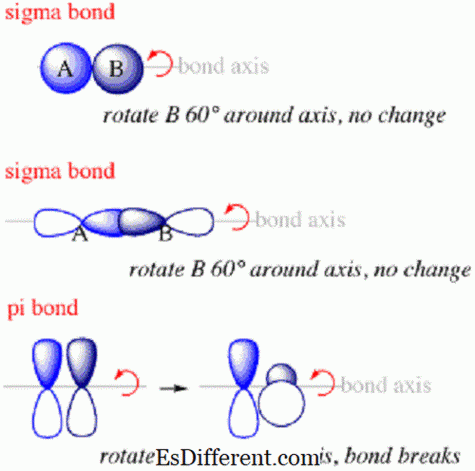
Bon pi adalah ikatan antara atom dalam molekul di mana elektron di atas dan di bawah paksi menyambung nukleus atom yang bergabung tetapi tidak di sepanjang paksi.Mereka adalah jenis ikatan kedua yang akan membentuk dalam molekul selepas ikatan sigma.
Pi bon dan
p orbital Sebab bahawa ikatan pi membentuk di atas dan di bawah paksi ikatan tetapi tidak di sepanjangnya adalah kerana ia biasanya terdiri daripada orbital yang bertindih seperti
p orbital pada atom terikat. Orbital ini tidak mempunyai ketumpatan elektron pada nukleus. Akibatnya, elektron-elektron yang membentuk bon pi yang terbentuk daripada orbital p yang bertindih akan sentiasa berkumpul di rantau yang tidak bersebelahan dengan nukleus. Bon pi juga boleh membentuk antara orbital atom lain, seperti orbital d yang mempunyai ciri-ciri yang sama dengan orbital p. Pi bon dan orbital pi
Apabila orbital
p atom berbeza bertindih, mereka membuat orbital pi molekul yang membolehkan ikatan pi diwujudkan. Ikatan ini boleh sekali lagi stabil atau tidak stabil bergantung kepada orbital di mana elektron terletak. Ikatan pi akan stabil jika lebih banyak elektron berada dalam orbital ikatan pi. Ia akan menjadi tidak stabil jika lebih banyak berada dalam orbital anti-ikatan atau jika nombor yang sama berada di kedua-duanya. Kesamaan antara ikatan sigma dan ikatan pi
Ikatan Sigma dan pi pi adalah kedua-duanya berdasarkan orbital molekul tertentu yang berasal dari tumpang tindih orbital atom tertentu, sebagai contoh, orbital
s dalam kes daripada ikatan sigma dan p orbital dalam kes bon pi. Mereka juga boleh stabil atau tidak stabil bergantung kepada sama ada elektron berada dalam orbital molekul ikatan atau orbital molekul anti-ikatan. Perbezaan antara ikatan sigma dan ikatan pi
Walaupun persamaan mereka, terdapat perbezaan yang penting.
Elektron yang membentuk ikatan sigma akan diagihkan di ruang sepanjang paksi yang menyambung nuklei bersambung sedangkan elektron di dalam ikatan pi akan diagihkan di atas dan di bawah paksi tetapi tidak di sepanjangnya.
- Ikatan Sigma adalah ikatan pertama untuk membentuk antara atom dalam molekul manakala ikatan pi adalah yang kedua.
- Ikatan Sigma sering terbentuk dengan gabungan orbital
- s dalam atom-atom yang berlainan manakala ikatan pi terbentuk dari gabungan p dan orbital yang serupa dalam atom-atom yang berlainan. Di samping itu, orientasi orbital yang bertindih yang membentuk ikatan pi akan berserenjang dengan orbitals bertindih yang membentuk ikatan sigma.
- Ikatan Sigma vs bon pi
Ikatan Sigma
| Pi pi | Orbital atom bertindih sepanjang paksi ikatan |
| Orbital atom bertindih di atas dan di bawah paksi ikatan | Ikatan pertama membentuk antara atom dalam molekul |
| Kedua-dua ikatan untuk membentuk antara atom dalam molekul | Dibentuk daripada orbital yang bertindih seperti orbital |
| s Dibentuk daripada orbital yang bertindih seperti orbital p | Orbital bertindih berserenjang dengan ikatan pi Orbital bertindih tegak dengan ikatan sigma |
| Ringkasan: Ikatan Sigma dan Pi | Ikatan sigma adalah ikatan antara atom dalam molekul yang sering terbentuk oleh |
s < Orbital 999 bertindih di sepanjang paksi yang menyambung nuklei bersambung.Ia adalah yang pertama membentuk dan kestabilannya bergantung kepada bagaimana elektron dibahagikan dalam orbitals ikatan dan antibonding ikatan. Bon pi adalah ikatan molekul yang sering terbentuk daripada orbital
p yang bertindih daripada atom yang berlainan. Elektron yang membentuk ikatan pi akan diagihkan di atas dan di bawah paksi yang menyambung nukleus atom terikat tetapi tidak di sepanjang paksi. Kestabilan ikatan ini juga bergantung kepada ikatan orbital pi dan antibonding. Bon Sigma akan menjadi bon pertama yang terbentuk dalam molekul manakala bon pi akan menjadi bon kedua untuk membentuk. Bon pi juga terbentuk daripada orbital atom yang berorientasikan serenjang dengan yang membentuk ikatan sigma.



