Perbezaan Antara EDTA dan EGTA
EDTA vs EGTA
EDTA dan EGTA kedua-duanya adalah agen chelating. Kedua-duanya adalah asid karboksilat poliamino dan mempunyai lebih kurang sifat yang sama.
EDTA
EDTA adalah nama yang dipendekkan untuk asid etilena diamine tetraacetic. Ia juga dikenali sebagai (etilena dinitrilo) asid tetraacetic. Berikut adalah struktur EDTA.
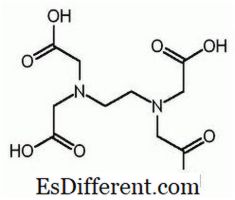
Molekul EDTA mempunyai enam tapak di mana ion logam boleh terikat. Terdapat dua kumpulan amino dan empat kumpulan karboksil. Dua atom nitrogen kumpulan amino mempunyai pasangan elektron yang tidak disertakan dalam setiap. EDTA adalah ligan heksadesentif. Juga, ia adalah agen chelating kerana keupayaan untuk menyerap ion-ion logam. EDTA membentuk chelates dengan semua kation kecuali logam alkali dan chelates ini cukup stabil. Hasil kestabilan dari beberapa tapak kompleks dalam molekul yang menimbulkan struktur sangkar seperti ion logam. Ini mengasingkan ion logam daripada molekul pelarut, sekali gus mencegah solvation. Kelompok carboxyl EDTA boleh memisahkan menderma proton; Oleh itu, EDTA mempunyai sifat asid. Pelbagai spesies EDTA disingkat sebagai H 4 Y, H 3 Y - , H 2 Y 2-, HY3 - dan Y 4- . Pada pH yang sangat rendah (medium berasid), bentuk protonasi EDTA (H 4 Y) adalah dominan. Sebaliknya, pada pH tinggi (medium asas), bentuk penuh deprotonasi (Y 4- ) mendominasi. Dan apabila perubahan pH dari pH rendah ke pH tinggi, bentuk EDTA lain mendominasi dalam nilai pH tertentu. EDTA boleh didapati sebagai bentuk proton atau sama ada garam. Disodium EDTA dan kalsium disodium EDTA adalah bentuk garam yang paling biasa. Asid bebas H 4 Y dan dihydrate garam natrium Na 2 H 2 Y. 2H 2 O boleh didapati secara komersial dalam kualiti reagen.
EGTA EGTA adalah istilah yang disingkat untuk asid etilena glikol tetraacetik. Ia adalah agen chelating, dan sangat mirip dengan EDTA.EGTA mempunyai pertalian yang lebih tinggi untuk ion kalsium daripada ion magnesium. EGTA mempunyai struktur berikut.
Seperti EDTA, EGTA juga mempunyai empat kumpulan karboksil, yang boleh menghasilkan empat proton apabila disosiasi. Terdapat dua kumpulan amina dan dua atom nitrogen kumpulan amino mempunyai pasangan elektron yang tidak disertakan dalam setiap. EGTA boleh digunakan sebagai penampan untuk menyerupai pH sel hidup. Properti EGTA ini membenarkan penggunaannya dalam Tandem Affinity Purification, yang merupakan teknik pemurnian protein.

Apakah perbezaan antara


