Perbezaan antara hidroksil dan hidroksida | Hydroxyl vs Hydroxide
Perbezaan Kunci - Hydroxyl vs Hydroxide
Kedua-dua istilah hidroksil dan bunyi hidroksida sangat serupa kerana kedua-duanya mempunyai dua atom yang sama, Oksigen (O = 16) H = 1). Hidroksida adalah ion negatif dengan cas tunggal dan hidroksil tidak terdapat dalam bentuk bebas, ia adalah sebahagian daripada molekul atau ion lain. Ion hidroksida lebih reaktif daripada kumpulan hidroksil dalam molekul. Ini adalah perbezaan utama antara hidroksil dan hidroksida.
Apakah itu Hydroxyl?
Hydroxyl adalah sebatian neutral dan ia adalah sebatian elektrik neutral ion hidroksida yang sama. Bentuk bebas hidroksil (• HO) adalah radikal dan apabila ia terikat kovalen kepada molekul lain ia dilambangkan sebagai kumpulan hidroksil (-OH). Kumpulan hidroksil boleh bertindak sebagai nukleofil dan radikal hidroksil digunakan sebagai pemangkin dalam kimia organik. Kumpulan hidroksil tidak sangat reaktif seperti nukleofil yang lain. Walau bagaimanapun, mereka adalah fasilitator dalam pembentukan daya intramolekul yang kuat yang dipanggil 'ikatan hidrogen'.

Apakah itu Hydroxide?
Hidroksida adalah anion diatomik yang mengandungi atom oksigen dan atom hidrogen. Ikatan antara oksigen dan atom hidrogen adalah kovalen dan formula kimianya ialah OH - . Pengionan air sendiri menghasilkan ion hidroksil dan oleh itu ion hidroksil adalah bahagian semula jadi di dalam air. Ion hidroksida digunakan sebagai asas, ligan, nukleofil dan pemangkin dalam tindak balas kimia. Di samping itu, ion hidrogen menghasilkan garam dengan kation logam dan kebanyakannya memisahkan dalam larutan akueus, melepaskan ion hidroksida terlarut. Banyak bahan kimia bukan organik mengandungi istilah "hidroksida" dalam nama mereka, tetapi mereka bukan ionik dan mereka adalah sebatian kovalen yang mengandungi kumpulan hidroksil.

Apakah perbezaan antara Hydroxyl dan Hydroxide?
Struktur:
Hidroksil: Hydroxyl adalah sebatian elektrik neutral yang boleh didapati dua cara, sebagai bentuk radikal dan kovalen.

Hidroksil radikal Apabila ia kovalen terikat kepada molekul
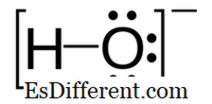
Hidroksida: Hidroksida adalah ion negatif dan caj negatif adalah pada atom oksigen.
Hydroxyl: Kumpulan hidroksil terdapat dalam sebatian organik; alkohol, asid karboksilat dan kumpulan hidroksil yang mengandungi gula. Sebatian yang mengandungi kumpulan hidroksil seperti air, alkohol, dan asid karboksilik boleh dengan mudah diganggu.Di samping itu, kumpulan hidroksil ini terlibat dalam pembentukan ikatan hidrogen. Bon hidrogen membantu molekul untuk melekat bersama dan ini membawa kepada pemilikan titik mendidih dan lebur yang lebih tinggi. Secara umum, sebatian organik tidak larut dalam air; molekul ini menjadi sedikit larut air apabila ia mengandungi dua atau lebih kumpulan hidroksil.
Hidroksida: Kebanyakan bahan kimia yang mengandungi hidroksida dianggap sangat menghakis, dan sesetengahnya sangat berbahaya. Apabila bahan kimia ini dibubarkan di dalam air, ion hidroksida bertindak sebagai asas yang sangat kuat. Oleh kerana ion hidroksida dikenakan caj negatif, ia sering terikat kepada ion positif yang dikenakan.
Sesetengah sebatian ionik yang mengandungi kumpulan hidroksida dalam molekul mereka dibubarkan dengan sangat baik dalam air; asas korosif seperti natrium hidroksida (NaOH) dan kalium hidroksida (KOH) boleh diambil sebagai contoh. Walau bagaimanapun, beberapa hidroksida lain yang mengandungi sebatian ionik tidak larut dalam air; Contohnya adalah tembaga (II) hidroksida [Cu (OH) 2 - berwarna biru terang] dan besi (II) hidroksida [Fe (OH) 2 - coklat].
Reaktiviti:
Hydroxyl : Kumpulan hidroksil kurang reaktif berbanding dengan kumpulan hidroksida. Tetapi, kumpulan hidroksil mudah membentuk bon hidrogen dan menyumbang untuk membuat molekul lebih larut dalam air.
Walau bagaimanapun, radikal hidroksil sangat reaktif dan sangat berguna dalam reaksi kimia organik.
Hidroksida: Kumpulan hidroksida (OH - ) dianggap sebagai nukleofil yang kuat dalam kimia organik.
Rujukan: Martin. chaplin @ btinternet. com, M. C. (n. d.). Ion hidroksida. Diambil pada 28 Disember 2016, dari siniHydroxide Ion: Definisi & Formula - Transkrip Video & Pelajaran. (n. d.). Diperolehi 28 Disember 2016, dari siniHydroxide. (n. d.). Diperoleh pada 28 Disember 2016, dari kumpulan Hydroxy ini. (n. d.). Diambil pada 28 Disember 2016, dari siniHydroxyl Group: Definisi, Struktur & Formula. (n. d.). Diperoleh pada 28 Disember 2016, dari sini H. (2014). Apakah Kumpulan Hydroxyl? Diperoleh pada 28 Disember 2016, dari sini



