Perbezaan Antara Acetaldehyde dan Acetone | Acetaldehyde vs Acetone
Perbezaan Utama - Acetaldehyde vs Acetone
Kedua-dua Acetaldehyde dan Acetone adalah molekul organik kecil, tetapi terdapat perbezaan di antara mereka berdasarkan kumpulan fungsinya. Dalam erti kata lain, mereka adalah dua sebatian karbonil yang berlainan dengan sifat kimia dan fizikal yang berlainan. Asetil adalah ahli terkecil daripada kumpulan ketone, sedangkan asetaldehida adalah kumpulan aldehid terkecil. Perbezaan utama antara Acetaldehyde dan Acetone ialah bilangan atom karbon dalam struktur; aseton mempunyai tiga atom karbon , tetapi asetaldehid mempunyai hanya dua atom karbon. Perbezaan dalam bilangan atom karbon dan mempunyai dua kumpulan berfungsi berbeza menyebabkan banyak perbezaan lain dalam sifatnya.
Apa itu Acetone?
Acetone adalah kumpulan terkecil ketone, juga dikenali sebagai propanone . Ia adalah cecair mudah terbakar, mudah terbakar, mudah terbakar yang digunakan sebagai pelarut. Kebanyakan pelarut organik tidak larut dalam air, tetapi aseton boleh larut dengan air. Ia sangat sering digunakan untuk tujuan pembersihan di makmal dan sebagai bahan aktif utama dalam cecair penghilang cat kuku dan dalam cat nipis.

Apakah Acetaldehyde itu?
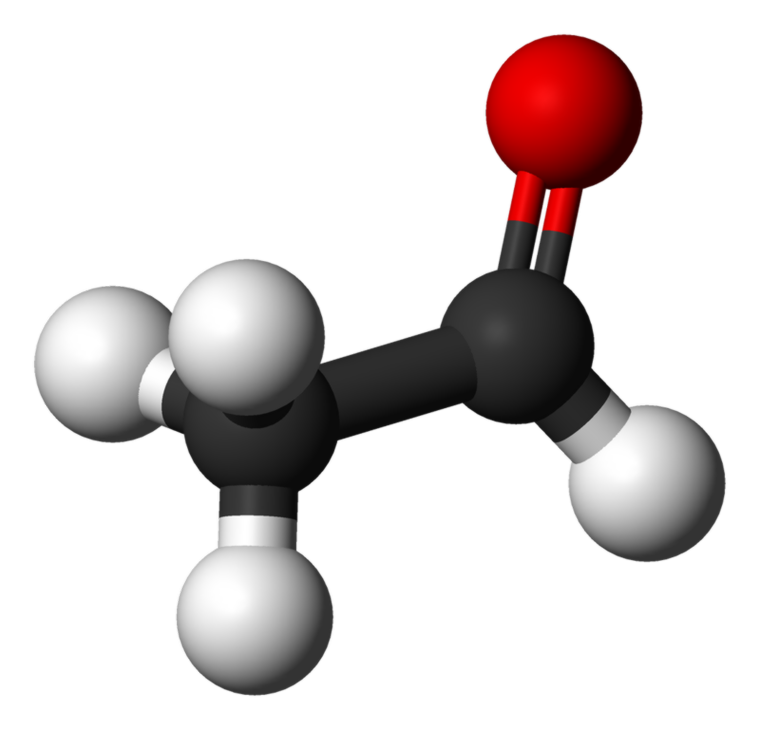
Acetaldehyde, juga dikenali sebagai etanal adalah kumpulan aldehid terkecil. Ia adalah cecair yang tidak berwarna dan mudah terbakar dengan bau yang kuat. Terdapat banyak kegunaan industri seperti menghasilkan asid asetik, minyak wangi, ubat-ubatan dan beberapa perisa.
Apakah perbezaan antara Acetaldehyde dan Acetone?
Struktur dan sifat-sifat umum Acetaldehyde dan Acetone
Acetone: Rumus molekul aseton C 3 H 6 O. Ia adalah ahli keluarga ketone yang paling mudah. Ia adalah cecair mudah terbakar yang mudah terbakar dengan bau yang pedas.

Acetaldehyde: Rumusan molekul asetaldehida C 2 H 4 O. Ia adalah yang paling mudah dan salah satu ahli yang paling penting dalam keluarga aldehida. Ia adalah cecair yang tidak berwarna, mudah terbakar, mudah terbakar pada suhu bilik.

Kejadian Acetaldehyde dan Acetone
Acetone: Secara amnya, aseton terdapat di dalam darah dan air kencing manusia. Ia juga dijana dan dilupuskan dalam tubuh manusia semasa metabolisme normal. Apabila orang mengalami kencing manis, ia dihasilkan dalam kuantiti yang lebih besar dalam tubuh manusia.
Acetaldehyde: Acetaldehyde secara semulajadi terdapat dalam pelbagai tumbuhan (kopi), roti, sayuran dan buah masak.Di samping itu, ia terdapat dalam asap rokok, gasolin dan ekzos diesel. Juga, ia adalah perantaraan dalam metabolisme alkohol.
Penggunaan Acetaldehyde dan Acetone
Acetone: Acetone terutamanya digunakan sebagai pelarut organik di dalam makmal kimia dan juga merupakan ejen aktif dalam menghasilkan penghilang kuku kuku dan nipis dalam industri cat.
Acetaldehyde: Acetone digunakan untuk mengeluarkan asid asetik, minyak wangi, pewarna, agen perasa dan ubat-ubatan.
Ciri-ciri Acetaldehyde dan Acetone
Pengenalan
Acetone: Acetone memberikan hasil positif untuk ujian iodoform. Oleh itu, ia boleh dengan mudah dibezakan daripada acetaldehyde menggunakan ujian iodoform.
Acetaldehyde: Acetaldehyde memberikan cermin perak kepada "reagen Tollen" manakala keton tidak memberikan hasil yang positif untuk ujian ini. Kerana, ia tidak boleh mengoksida dengan mudah. Ujian asid krom dan reagen Fehling juga boleh digunakan untuk mengenal pasti asetaldehida.
Reaktiviti
Kereaktifan kumpulan karboksil (aldehid dan keton) terutamanya disebabkan oleh kumpulan karbonil (C = O).
Aseton: Secara amnya, kumpulan alkil adalah kumpulan sumbangan elektron. Asetil mempunyai dua kumpulan metil dan mengurangkan polarisasi kumpulan karbonil. Oleh itu, ia menjadikan sebatian kurang reaktif. Dua kumpulan metil yang melekat pada kedua-dua belah kumpulan karbonil membawa kepada halangan yang lebih banyak juga. Oleh itu, aseton kurang reaktif daripada asetaldehida.
Acetaldehyde: Sebaliknya, asetaldehida hanya mempunyai satu kumpulan metil dan satu atom hidrogen yang melekat pada kumpulan karbonil. Sebagai kumpulan metil menyumbang elektron, atom hidrogen menarik elektron; ini menjadikan molekul lebih polarisasi, dan ia menjadikan molekul lebih reaktif. Berbanding dengan aseton, asetaldehida mempunyai kesan kurang stearic, dan molekul lain boleh mendekati dengan mudah. Disebabkan oleh sebab-sebab ini, asetaldehid lebih reaktif daripada aseton.