Perbezaan Antara Lysine dan L-lysine | Lysine vs. L-lysine
Perbezaan Utama - Lysine vs L-lysine
Lysine dan L-lisin adalah kedua-dua jenis asid amino, beberapa perbezaan di antara mereka. Perbezaan utama antara Lysine dan L-lysine adalah keupayaan untuk memutarkan cahaya polarisasi pesawat. Lysine adalah asid α-amino penting secara aktif secara biologi. Ia boleh berlaku dalam dua bentuk isomerik kerana kemungkinan membentuk dua enantiomer berbeza di sekitar atom karbon chiral. Ini dikenali sebagai bentuk L- dan D-, sama dengan konfigurasi tangan kiri dan kanan. Formula L- dan D ini dikatakan aktif secara optik dan memutarkan cahaya polarisasi pesawat dalam erti kata yang berbeza; mengikut arah jam atau lawan jam. Sekiranya cahaya berputar lisin mengikut lawan jam, maka cahaya memperlihatkan levorotation, dan ia dikenali sebagai L-lisin. Walau bagaimanapun, ia perlu diperhatikan dengan teliti di sini bahawa pengekalan D- dan L bagi isomer tidak sama dengan d-dan l-label.
Apa itu Lysine?
Lysine adalah asid amino penting yang tidak disintesis dalam tubuh kita dan harus dibekalkan oleh diet biasa. Oleh itu, lisin adalah asid amino penting bagi manusia. Ia adalah sebatian organik yang terdiri daripada amina (-NH 2 ) dan kumpulan berfungsi asid carboxylic (-COOH) dengan rumus kimia NH 2 - (CH 2) 4 -CH (NH 2 ) - COOH. Unsur utama lisin adalah karbon, hidrogen, oksigen, dan nitrogen. Dalam biokimia, asid amino yang mempunyai kedua-dua amina dan kumpulan asid karboksilik yang dilampirkan pada atom karbon pertama (alpha-) dikenali sebagai α-amino acids . Oleh itu, lisin juga dianggap sebagai asid α-amino. Struktur lisin diberikan dalam rajah 1.
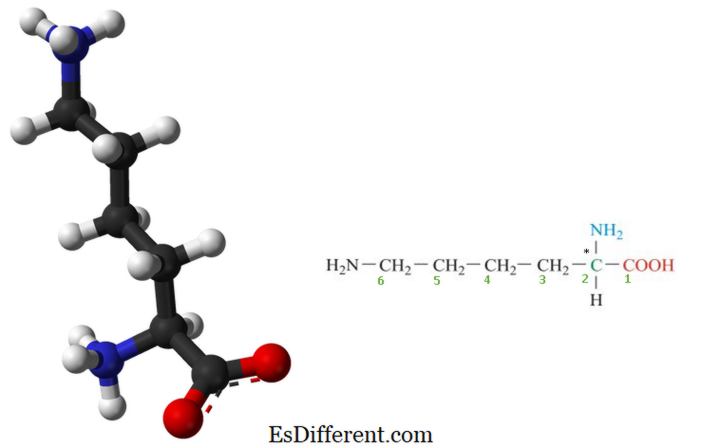
Lysine adalah asas dalam kerana ia mengandungi dua amino asas kumpulan dan satu kumpulan asid karboksilik. Oleh itu, ia juga membentuk ikatan hidrogen yang luas kerana terdapat dua kumpulan amino.
Sumber lysine yang baik adalah sumber haiwan kaya protein seperti telur, daging merah, kambing, daging babi, dan ayam, keju, dan ikan tertentu (seperti ikan kod dan sarden). Lysine juga kaya dengan protein tumbuhan seperti soya, kacang, dan kacang. Walau bagaimanapun, ia adalah pengambilan asid amino dalam kebanyakan bijirin bijirin tetapi banyak terdapat dalam kebanyakan denyut dan kekacang.
Lysine mempunyai empat kumpulan yang berbeza di sekitar 2
nd karbon, dan ia struktur asimetri .Juga, lisin adalah asid amino optik aktif kerana kehadiran atom karbon asimetrik atau kiral ini. Oleh itu, lysine boleh menghasilkan stereoisomer yang merupakan molekul isomerik yang mempunyai rumus molekul yang sama, tetapi berbeza dalam orientasi tiga dimensi atom-atom mereka di angkasa. Enantiomer adalah dua stereoisomer yang berkaitan dengan satu sama lain oleh refleksi atau mereka cermin imej antara satu sama lain yang tidak superimposable. Lysine terdapat dalam dua bentuk enantiomer yang dikenali sebagai L- dan D- dan enantiomer lisin diberikan dalam Rajah 2. Rajah 2: Enantiomer asid amino lisin. Kumpulan-kumpulan COOH, H, R dan NH2 disusun di sekitar atom C dengan cara yang mengikut arah jam, enantiomer dipanggil L-bentuk dan D-bentuk sebaliknya. L- dan D- merujuk kepada susunan ruang di sekitar atom karbon dan tidak merujuk kepada aktiviti optik. Sedangkan bentuk L- dan D- dari molekul kiral akan memutar pesawat cahaya terpolarisasi dalam arah yang berbeza, sesetengah bentuk L (atau bentuk D) berputar cahaya ke kiri (levo atau l-) dan beberapa ke kanan (dextro atau bentuk d). l- dan bentuk d- dipanggil isomer optik.

L-lisin dan D-lisin adalah enantiomer antara satu sama lain mempunyai ciri-ciri fizikal yang sama, kecuali arah di mana mereka memutar cahaya terpolarisasi. Mereka mempunyai hubungan imej cermin bukan superimposable. Walau bagaimanapun, tatanama D dan L tidak biasa dalam asid amino termasuk lisin. Mereka memutarkan cahaya polarisasi pesawat dalam magnitud yang sama tetapi dalam arah yang berbeza. D dan L-isomer lysine yang memutarkan cahaya terpolarisasi pesawat dalam arah arah jam dipanggil sebagai dextrorotatory atau
d-lysine dan yang memutar cahaya polarisasi pesawat dalam arah lawan arah jam dipanggil sebagai laevorotatory atau L-lysine (Rajah 2). L-Lysine ialah
bentuk stabil lysine yang paling banyak terdapat. D-Lysine adalah bentuk sintetik lisin dan boleh disintesis dari l-lisin oleh rasa bersemangat. Ia digunakan dalam pemprosesan poli-d-lisin, yang digunakan sebagai bahan lapisan untuk meningkatkan lampiran sel. L-Lysine memainkan peranan penting dalam tubuh manusia, dalam penyerapan kalsium, pembangunan protein otot, dan sintesis hormon, enzim, dan antibodi. Secara industri, L-lisin dihasilkan oleh proses fermentasi mikrob menggunakan Corynebacterium glutamicum. Apakah perbezaan antara Lysine dan L-lysine?
Lysine dan L-lysine mempunyai sifat fizikal yang sama, kecuali arah di mana mereka memutarkan cahaya terpolarisasi. Akibatnya, L-lisin mungkin mempunyai kesan biologi yang sangat berbeza dan ciri-ciri fungsian. Walau bagaimanapun, penyelidikan yang sangat terhad telah dilakukan untuk membezakan kesan-kesan biologi dan ciri-ciri fungsian ini. Sesetengah perbezaan ini termasuk,
Rasa
L-lisin:
L-bentuk asid amino cenderung tidak enak. D-lisin:
D-bentuk asid amino cenderung rasa manis. Oleh itu l-lisin mungkin kurang / tidak lebih manis daripada lisin.
Kelimpahan
L-lysine:
Asid amino l termasuk l-lisin adalah bentuk yang paling melimpah di alam.Sebagai contoh, sembilan daripada sembilan belas asid L-amino yang terdapat dalam protein adalah dextrorotatory dan selebihnya adalah levorotatory. D-lisin:
Bentuk asid amino D yang diamati secara eksperimen didapati jarang berlaku. Rujukan: Solomons, T. W. Graham, dan Graig B. Fryhle (2004). Kimia Organik (8
th ed). Hoboken: John Wiley & Sons, Inc. Everhardus, A. (1984). Stereokimia, asas karut canggih dalam farmakokinetik dan farmakologi klinikal, Jurnal Eropah Farmakologi Klinik, 26 , 663-668. Image Courtesy: "L-lysine-monocation-from-hydrochloride-dihydrate-xtal-3D-ball" oleh Ben Mills - Kerja sendiri melalui Wikimedia Commons


